Tendances
Publié le 10 juil 2023Lecture 16 min
Traitements intra-artériels des métastases hépatiques de tumeurs neuroendocrines
Maxime RONOT1*, Lambros TSÉLIKAS2*, Paris et Villejuif
Les néoplasies neuroendocrines sont diverses tumeurs développées au dépend du système neuroendocrinien diffus. L'Organisation Mondiale de la santé (OMS) classe ces néoplasies en fonction de leurs caractéristiques morphologiques (différenciation) et de leur degré de prolifération, évalué par l’index mitotique ou le Ki-67. Les tumeurs bien différenciées sont appelées « tumeurs neuroendocrines » (TNE) alors que les tumeurs peu ou pas différenciées sont appelées « carcinomes neuroendocrines » (CNE). Parmi les TNE, on distingue les lésions de grade (G) 1, 2 et 3 selon leur degré de prolifération(1).
Les TNE sont métastatiques au moment du diagnostic dans environ 20 %, 30 % et 50 % des tumeurs G1,G2 et G3, respectivement, le statut métastatique (tableau 1) représentant le facteur pronostique le plus important après le grade tumoral(2,3). En effet, la survie à 5 ans est estimée à 13-54 % en cas de métastases, contre 75-99 % en leur absence(3). Le foie constitue le site métastatique le plus fréquent, surtout pour les TNE d’origine gastro-entéro-pancréatique (GEP-NET).
*TNE : tumeur neuroendocrine ; CNE : carcinome neuroendocrine.
*L’index mitotiques doit être exprimé comme le nombre de mitoses/2 mm2 tel que déterminé en comptant dans 50 champs de 0,2 mm2 (c’est-à-dire dans une surface totale de 10 mm2). La valeur de l’indice de prolifération Ki-67 est déterminée en comptant au moins 500 cellules dans les régions de marquage le plus élevé (points chauds). Le grade final est celui donné par l’un des deux indices de prolifération qui place la néoplasie dans la catégorie de grade supérieur.
**Les CNE peu différenciés ne sont pas officiellement gradés, mais sont considérés comme de haut grade par définition.
***Dans la plupart des tumeurs mixtes endocrines, les composants neuroendocriniens et non neuroendocriniens sont peu différenciés et le composant neuroendocrinien un indice de prolifération du même ordre que le composant non endocrinien. Toutefois, un ou deux composants peuvent être bien différenciés. Lorsque cela est le cas, chaque composante doit donc être évaluée séparément.
Selon les recommandations de l’European NeuroEndocrine Tumors Society (ENETS)(4), les tumeurs bien différenciées, surtout de grade 1 ou 2, sont candidates à des thérapies locorégionales hépatiques, en particulier lorsque la maladie hépatique est isolée ou dominante. Les traitements locorégionaux comprennent la chirurgie (résection et transplantation), et les thérapies guidées par l’image (ablation et traitements intra-artériels hépatiques). Dans ces derniers, on inclut les chimioembolisations, l’embolisation et la radioembolisation.
Cette mini revue discute les avantages et les risques des traitements intra-artériels hépatiques, et présente leurs principaux résultats oncologiques pour le traitement des métastases hépatiques de TNE. Les ablations tumorales se seront pas abordées.
Justification des traitements intra-artériels hépatiques
La justification des traitements intra-artériels hépatiques repose sur la différence d’apport vasculaire du foie et des métastases. Environ 70 % de l’apport sanguin du foie provient de la veine porte, alors que les métastases hépatiques sont alimentées exclusivement par l’artère hépatique. Ainsi, les traitements intra-artériels qui peuvent comprendre l’embolisation de branches artérielles, l’injection de drogues de chimiothérapie ou encore d’une forte dose de radiothérapie ciblent de manière préférentielle les métastases. Ceci permet en théorie d’améliorer l’efficacité anti-tumorale des traitements tout en améliorant leur profil de toxicité.
Éléments techniques
Les traitements intra-artériels hépatiques sont le plus souvent réalisés au cours d’une courte hospitalisation, sous une légère sédation ou une anesthésie locale chez des patients ayant reçu une antalgie préventive et une anxiolyse. L’abord est artériel fémoral droit ou, de plus en plus souvent, radiale gauche.
Le premier temps de tous les traitements est la réalisation d’une angiographie hépatique en deux (angiographie sous-traite numérisée) et trois dimensions (imagerie type cone-beam ou artério-scanner) permettant d’apprécier l’anatomie artérielle de chaque patient. Les images obtenues ont un double rôle de ciblage (sélection des artères qui alimentent les tumeurs à traiter) et de guidage (contrôle en temps réel de la progression du matériel endovasculaire). Les traitements diffèrent entre eux par la nature du traitement injecté (figure 1).
Figure 1. Illustration des étapes d’une prise en charge par traitement intra-artériel hépatique. pancréatique localement avancé.
Le diagramme en haut (A) illustre le calendrier de la prise en charge et le schéma du bas (B) détaille les différentes étapes techniques d’une séance de traitement.
CB-CT « cone beam computed tomography », acronyme anglais pour imagerie tomographique à faisceau conique qui correspond à l’imagerie 3D ; Ho166 : holmium 166 ; RCP : réunion de concertation pluridisciplinaire ; RI : radiologie interventionnelle, SIRT « selective internal radiation therapy », acronyme anglais de la radioembolisation, Y90 : yttrium 90.
La chimioembolisation comprend l’injection d’un médicament de chimiothérapie et une embolisation des artères ciblées. Lorsque le médicament est injecté sous forme d’émulsion dans de l’huile de pavot (lipiodol, Guerbet), on parle de chimioembolisation conventionnelle. La radio-opacité de l’huile permet un contrôle radioscopique de l’injection et sert de vecteur au médicament. Cette propriété de vectorisation permet de diminuer l’exposition systémique et d’augmenter la concentration hépatique, surtout dans les tumeurs (jusqu’à 100 fois plus que celle obtenue par une injection par voie intraveineuse). Les drogues utilisées dans la chimioembolisation sont variées. La grande majorité des équipes utilise la doxorubicine à des doses de l’ordre de 1 mg/kg, mais d’autres équipes utilisent une combinaison de cisplatine, doxorubicine et mitomycine C. La strep-tozotocine est également utilisée, car elle aurait une efficacité plus grande que la doxorubicine. Il faut toutefois noter que son injection nécessite une anesthésie générale en raison d’une douleur importante lors de l’injection intra-artérielle hépatique induite par un pH acide. Plus récemment, l’oxaliplatine a été rapportée comme potentiellement intéressante.
L’embolisation simple est, comme son nom l’indique, une embolisation ciblée des vaisseaux alimentant les tumeurs, sans injection de drogue de chimiothérapie.
La radioembolisation est, quant à elle, une radiothérapie sélective interne vectorisée. Elle consiste en l’injection de microbilles calibrées biocompatibles mais non biodégradables de résine ou de verre, associées à une radio-isotope émetteur b négatif. L’isotope est le plus souvent l’yttrium-90 (90Y), mais de nouvelles plateformes utilisant l’holmium-166 (166Ho) sont disponibles. La séance de traitement proprement dite est précédée d’une première artériographie dite de « simulation » réalisée 7-14 jours. Au cours de celle-ci, une activité d’environ 500 MBq est injectée dans la zone à traiter sous la forme de macro-agrégats d’albumine humaine (MAA) marqués au technétium 99 méta-stable (99mTc). Celle-ci permet de réaliser une scintigraphie pour estimer la fraction de shunt pulmonaire (dose maximale tolérable au poumon d’environ 30 Gy), vérifier l’absence de perfusion extra-hépatique et pour calculer la dose estimée à la tumeur et au foie non tumoral (dosimétrie personnalisée). La réponse tumorale est fortement associée à la dose tumorale absorbée, et la toxicité hépatique à la dose reçue au foie non tumoral, et au foie non ciblé. Les métastases hépatiques traitées sont le plus souvent diffuses ou bilobaires. Le traitement par voie intra-artérielle de toute la charge tumorale requiert généralement deux ou trois séances de traitement administrées séquentiellement avec 4 à 8 semaines d’intervalle, pour améliorer l’efficacité en limitant la toxicité. Si les tumeurs sont en petit nombre, un cathétérisme sélectif d’une ou des artères vascularisant les tumeurs est réalisé.
Sélection des patients
Les patients ayant une maladie hépatique prédominante, évolutive (même lentement), non résécable ou des symptômes majeurs mal contrôlés sont les meilleurs candidats pour les traitements intra-artériels hépatiques. La présence de métastases pulmonaires, ganglionnaires ou osseuses de faible volume n’est pas une contre-indication absolue. Parmi ces patients, les meilleurs candidats sont ceux ayant une charge tumorale limitée (< 30 %), faites de métastases de TNE de l’intestin moyen, de bas grade, hyper-rehaussées au temps artériel en imagerie. L’insuffisance hépatique est une contre-indication commune à tous les traitements intra-artériels. L’ictère obstructif et les anastomoses bilio-digestives sont surtout contre-indiqués en cas de chimioembolisation ou d’embolisation, car ils exposent à des complications infectieuses à type de cholangite, de nécrose des voies biliaires ou d’abcès hépatique. La radioembolisation serait moins problématique, l’effet emboligène étant moindre du fait de la taille et du nombre de billes injectées, même si le risque n’est pas nul. Une thrombose de la veine porte et l’insuffisance rénale sont également des contre-indications relatives. Les patients présentant une atteinte de plus de 75 % du volume hépatique doivent être traités avec une grande prudence, en ciblant quelques segments du foie à la fois. Enfin, notons des contre-indications liées aux drogues utilisées, une fraction d’éjection < 50 % en cas d’utilisation de la doxorubicine et une protéinurie en cas d’utilisation de la strep-tozocine.
Après un traitement intra-artériel (qui comme nous l’avons dit est souvent fractionné), l’usage est d’évaluer le patient. Cette évaluation est réalisée 4-6 semaines après le traitement pour les chimio-embolisations ou embolisations, et à 3 mois pour la radioembolisation. Les traitements ultérieurs sont délivrés en fonction de la tolérance au traitement, du temps nécessaire pour que la fonction hépatique revienne à la valeur initiale, de la réponse clinique et de la réponse tumorale dans les territoires traités. En cas de réponse jugée satisfaisante (réponse clinique et biologique, réponse objective en imagerie), il est souvent décidé d’attendre. Un nouveau traitement intra-artériel sera discuté en cas de progression de la maladie (clinique et ou radiologique) jugée techniquement accessible par voie intra-artérielle. En cas de progression non traitable par une telle approche (progression extra-hépatique, réseau artériel dégradé, toxicité jugée trop grande), une autre option thérapeutique est préférée.
Résultats
Les traitements intra-artériels font partie des traitements les plus efficace contre la maladie métastatique hépatique. La majorité de la littérature disponible concerne la chimioembolisation et l’embolisation qui sont des traitements plus anciens que la radioembolisation(5-8). Une réponse clinique (efficacité sur le syndrome sécrétoire) est obtenue chez 89 % (42-100 %) des patients avec une durée de réponse souvent supérieure à 12 mois(9-10). La réponse symptomatique est plus élevée lorsque le traitement est utilisé en première intention avec 70 % de réponse symptomatique complète et 20 % de réponse partielle. Sur le plan radiologique, une réponse objective est rapportée dans 58 % (11-89 %), avec ici encore un bénéfice plus grand lorsque le traitement est appliqué en première ou deuxième ligne (figure 2). Dans notre expérience, la survie sans progression hépatique médiane est de l’ordre de 16-20 mois. Les valeurs de survie globale rapportées dans la littérature sont quant à elle de l’ordre de 3 à 4 ans(11-13), jusqu’à 5 ans dans notre expérience. L’amélioration de la survie rapportée par les études les plus récentes témoigne sans doute d’une meilleure sélection des patients (traitement des tumeurs G1 et G2 uniquement, réalisé au début de la maladie) et d’une amélioration technique (cathéters, imagerie 3D).
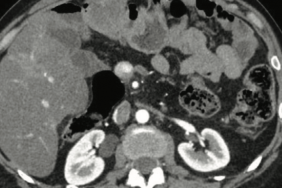
Figure 2. Exemples de chimioembolisation et d’embolisation de métastases hépatiques de tumeurs neuroendocrines. La ligne du haut montre le cas d’un patient de 52 ans ayant des métastases d’une TNE pancréatique de grade 1, responsables d’un envahissement d’environ 50 % du foie (A) traitées par chimioembolisation. L’indication de la chimioembolisation était posée devant une progression des lésions sous analogues de la somastostatine. Deux séances de chimioembolisation utilisant la streptotozocine ont été réalisées, permettant d’obtenir une réponse objective (B). Les séances ont été marquées par un syndrome post-embolisation modéré. La ligne du bas montre le cas d’un patient de 48 ans ayant des métastases d’une TNE intestinal de grade 1, responsables d’un envahissement d’environ 50 % du foie (C) traitées par embolisation. L’indication de l’embolisation était également posée devant une progression des lésions sous analogues de la somastostatine. Deux séances d’embolisation simple utilisant de la gélatine ont été réalisées, permettant d’obtenir une réponse complète (D). Les séances ont été marquées par un syndrome post-embolisation modéré.
Les facteurs prédictifs individuels de réponse ou de survie sont encore mal connus. Retenons toutefois le grade tumoral, le site de la tumeur primitive (meilleurs résultats observés dans les tumeurs de l’intestin moyen), la charge tumorale, l’étendue de la maladie extra-hépatique et l’existence de lignes de traitements antérieurs. Notons enfin que la profondeur de la réponse tumorale en imagerie est associée à la survie sans progression et à la survie globale.
Une revue rétrospective multicentrique comprenant 244 patients traités avec 273 radioembolisations a rapporté une amélioration des symptômes chez 79 % des patients (résolution 35 %, amélioration 44 %), et des taux de réponse objective et de contrôle de la maladie de 62,9 % et 91,4 %, respectivement (selon les critères mRECIST)(14). Deux métaanalyses récentes sont venues confirmer ces résultats, avec des taux de réponse objective et de contrôle tumorale de 50-51 % et 86 %, et une survie globale médiane de 28,5-32 mois(15,16). L’efficacité de la radioembolisation semble ainsi proche de celle rapportée pour la chimioembolisation ou l’embolisation (figure 3).
Figure 3. Exemple de radioembolisation réalisée chez une patiente de 45 avec métastases hépatiques d’une tumeur neuroendocrine pancréatique réséquée dix-sept ans plus tôt par duodéno-pancréatectomie céphalique. Les métastases étaient bilobaires et ont été traitées par deux séances de radioembolisation (microsphères de résines, Yttrium 90). La colonne de gauche (A-C) montre le scanner de baseline, la colonne du milieu (D-F) le ciblage par imagerie nucléaire et la colonne de droite (G-I), la réponse objective maintenue à 2 ans. La patiente n’a pas rapporté d’événement indésirable.
Toxicité et tolérance
À court terme, l’effet secondaire systémique le plus courant de la chimioembolisation ou de l’embolisation est le syndrome post-embolisation, qui associe fatigue, fièvre, douleur, nausées, vomis- sements, hyperleucocytose, hyperthrombocytose, cytolyse et légère augmentation du taux de bilirubine sérique. Le syndrome post-embolisation est très fréquent et serait mieux prévenu par l’administration d’ondansétron 30 minutes avant le traitement. Le contrôle de la douleur repose sur les antalgiques de pallier 1 à 3, selon une approche personnalisée. La plupart du temps, le syndrome post-embolisation est autolimité, s’améliorant en 3 à 5 jours avec une prise en charge médicale simple. Le passage systémique de la doxorubicine est responsable de vomissement et de nausées, tandis que l’alopécie est très inhabituelle. Une crise carcinoïde aiguë peut être déclenchée par ces traitements et, par conséquent, l’utilisation prophylactique d’analogues de la somatostatine est recommandée chez les patients présentant des tumeurs fonctionnellement actives. Chez ces patients, le dépistage et le traitement de la cardiopathie carcinoïde sont nécessaires avant chimioembolisation, notamment si une anthracycline est utilisée.
Sur le plan plus locale, la toxicité de la chimioembolisation et de l’embolisation est surtout hépato-biliaire, avec un risque de lésion atteignant 20 à 25 %. Ces lésions comprennent des dilatations biliaires, des sténoses ou thromboses portes, la survenue de bilome, voire de nécrose hépatique. Dans la grande majorité des cas, ce sont des atteintes modérées et infracliniques (figure 4).
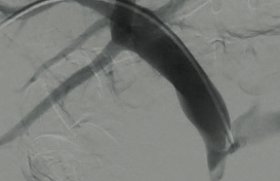
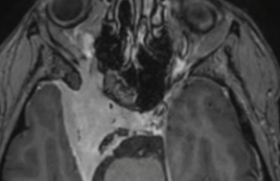
Figure 4. Exemple de toxicité hépatobiliaire chez un patient de 54 ans avec une tumeur neuroendocrine iléale grade 2. Antécédent d’hépatectomie droite pour métastases et de résection de la tumeur primitive. L’IRM (A) met en évidence une récidive des métastases dans le foie restant, apparaissant sous forme de blushs tumoraux sur les images d’angiographie soustraite (B). Le patient a été traité par deux séances de chimioembolisation conventionnelle (doxorubicine et lipiodol) et par une séance de chimioembolisation aux billes chargées à la doxorubicine. Dans les suites, le patient a développé une dilatation minime des voies biliaires puis un bilome sectoriel postérieur (C), communiquant avec les voies biliaires (D). Le traitement a consisté en la mise en place de drains biliaires percutanés et d’un drainage du bilome (E) qui ont permis la résolution des lésions (F).
La tolérance précoce de la radioembolisation est significativement meilleure. Une fatigue modérée est fréquente et le syndrome post-embolisation inexistant. Pour la très grande majorité des patients, la qualité de vie est peu ou pas altérée et revient à son état de base en 3-4 semaines. Des complications à type d’ulcère peuvent survenir en cas d’admi- nistration du traitement dans des artères à destinée extra-hépatiques (gastroduodénale, gastrique droite, falciforme, branches pancréatico-duodénales, etc.). Des cas de pneumopathies radiques ont été rapportés en cas de shunt pulmonaire majeure, ainsi que de décompensation hépatique précoce en cas de traitement d’un gros volume de foie chez des patients ayant une fonction hépatique altérée. C’est le rôle de la phase de simulation que d’anticiper et d’éliminer le risque de telles complications qui deviennent exceptionnelles dans les centres experts.
À plus long temps, la radioembolisation expose à un risque d’hépatopathie post-radique (dysmorphie type cirrhotique, ascite, splénomégalie, shunts porto-systémiques), ce d’autant que les traitements ont été bilobaires(17,18). Ceci peut conduire à des tableaux cliniques de décompensation hépatique. Ainsi, Curie et coll. ont récemment rapporté des taux de toxicité à long terme similaire entre chimioembolisation et radioembolisation (respectivement 22 % et 29 %), mais un taux de toxicité attribuable au traitement plus élevé en cas de radioembolisation (14 % contre 3 %)(19). Ainsi, la toxicité retardée associée à la chimioembolisation est en moyenne moins sévère et se manifeste principalement par des anomalies des tests hépatiques, alors que c’est la décompensation hépatique clinique qui domine en cas de radioembolisation. Une approche plus sélective, en épargnant des segments hépatiques et une analyse dosimétrique aussi bien des tumeurs que du parenchyme non tumoral, peuvent diminuer l’exposition hépa-ique, et donc le risque d’hépatopathie radio-induite.
Quel traitement intra-artériel ?
En l’absence d’études comparatives randomisées, il n’y a, aujourd’hui, pas d’argument solide pour choisir entre les différents traitements intra-artériels disponibles. La chimioembolisation conventionnelle (utilisant le lipiodol) et l’embolisation sont historiquement les traitements les plus utilisés et pour lesquels le plus de données sont disponibles.
Chimioembolisation ou embolisation ?
Le bénéfice de la chimioembolisation par rapport à l’embolisation simple n’a pas été démontré. Des données précliniques indiquent un possible bénéfice de la chimioembolisation. Des données cliniques historiques sur le traitement des métastases hépatiques de TNE ont rapporté une amélioration des taux de réponse objective et de survie lorsque la chimiothérapie administrée par voie IV était associée à une ligature artérielle hépatique. Gupta et coll. ont rapporté une absence de valeur ajoutée de la chimioembolisation chez les patients atteints de tumeurs de l’intestin moyen, mais un possible bénéfice en cas de tumeur primitive pancréatique (même si ces différences n’étaient pas statistiquement significatives) et ce, au prix d’une toxicité similaire(13). Le seul essai prospectif randomisé comparant chimioembolisation et embolisation ne comprenait que 26 patients inclus sur une période de 6 ans et ne démontrait aucune différence entre les deux traitements selon le critère d’évaluation principal (survie sans progression à 2 ans), avec des taux de réponse de 38 et 44 %, et des taux de contrôle de la maladie de 100 % et 92 %, respectivement(20).
Retenons donc qu’en raison de la petite taille et de la grande hétérogénéité des études, quasiment toutes rétrospectives, il semble exister une tendance à la supériorité de la chimioembolisation conventionnelle sur l’embolisation, avec un bénéfice qui semble plus important pour les métastases de TNEpancréatiques. Cette tendance ne s’accompagne d’aucune différence de toxicité.
Chimioembolisation conventionnelle ou aux billes chargées ?
Le chimioembolisation utilisant les billes chargées est théoriquement séduisante car elle permet de réaliser en un seul temps l’injection de la drogue de chimio-thérapie et l’embolisation. Des données précliniques ont montré une meilleure exposition tumorale aux drogues de chimiothérapie au prix d’un passage systémique faible. Les premières publications utilisant les billes chargées pour le traitement des métastases hépatiques de TNE montraient un taux de réponse élevé, entre 57 à 80 % selon les critères mRECIST, avec un temps de progression de 14-15 mois(21,22). Toutefois, plusieurs études ont depuis lors rapporté une augmentation significative de la toxicité hépatobiliaire locale en comparaison à la chimioembolisation conventionnelle(23). Baghat et coll. ont ainsi rapporté une analyse intermédiaire chez 13 patients atteints de métastases hépatiques de TNE dans le cadre d’un essai de phase II(24). Malgré un taux de réponse encourageant de 78 %, sept patients ont développé des bilomes (54 %) et quatre patients ont eu un drainage percutané conduisant à l’interruption de l’essai. Retenons donc qu’en l’absence d’essais cliniques randomisés, il est conseillé d’utiliser la chimioembolisation conventionnelle, en particulier lorsque l’ensemble du foie doit être traité. Le choix de la radioembolisation Comme nous l’avons vu, la radioembolisation présente un profil de toxicité bien meilleur dans la période post-traitement précoce, mais l’irradiation du foie sain rend le traitement moins répétable que les chimioembolisations/embolisations en raison du risque d’hépatopathie radique retardée.
Retenons donc qu’à ce jour, la radioembolisation est le plus souvent considérée chez les patients ayant été traités par chimioembolisation ou embolisation sans succès ou chez ceux ayant des contre-indications (ou étant considérés à risque) à la chimioembolisation, notamment les thromboses porte majeure, les anastomoses bilio-digestives ou une faible fraction d’éjection cardiaque.
Conclusion et perspectives
En raison de sa complexité, la maladie métastatique hépatique d’origine neuro-endocrine doit être prise en charge dans des centres experts. Dans l’arsenal thérapeutique disponible, la radiologie interventionnelle fournit un ensemble de traitements intra-artériels (chimioembolisation, embolisation ou radioembolisation) adaptés aux patients ayant une maladie hépatique isolée ou dominante. Ils sont associés à une très bonne efficacité clinique et symptomatique, des taux de réponse objective élevés au prix d’une toxicité acceptable, principalement locale.
Le choix du traitement intra-artériel n’est pas standardisé et doit s’inscrire dans une stratégie plus large chez ces patients souvent multitraités sur de longues périodes. De futures études randomisées évaluant le bénéfice relatif en termes d’efficacité et de toxicité des différents traitements intra-artériels disponibles paraissent essentielles pour un meilleur contrôle de la maladie. De même, essentielle est leur évaluation en termes de stratégie, seule ou en combinaison avec les autres thérapies systémiques et locales administrées de manière séquentielle ou concomitante. Parmi celles-ci, la combinaison avec les molécules immunomodulatrices ouvre des perspectives et devra obtenir notre plus grande attention.
* 1 Service de radiologie, AP-HP Nord, hôpital Beaujon, Clichy ; Université de Paris ; Inserm UMR 1149, CRI, Paris
2 Service d'imagerie thérapeutique, Gustave-Roussy, Villejuif ; Université de Paris Saclay, Saint-Aubin ; Laboratoire de Recherche Translationnelle en Immunothérapie (LRTI), Inserm U1015, Gustave-Roussy, Villejuif.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :