C Demain
Publié le 10 juil 2023Lecture 9 min
Thermoablation des tumeurs hépatiques centrales sur coussin d’air ambiant ou aérothermoablation - Pourquoi ? Comment ? Et quels résultats ?
Patrick CHEVALLIER, Manuel GARGIULO, Mohamed EL ZIBAWI, Ines ORENSTEIN, Antony SCHEIT, Olivier LOPEZ, Centre d’imagerie interventionnelle oncologique et viscérale, hôpital Archet II, Centre hospitalier et universitaire de Nice
Le traitement par thermoablation percutanée des tumeurs hépatiques s'est développé depuis les années 1990, en ayant démontré une grande efficacité pour des tumeurs mesurant moins de 3 à 4 cm de diamètre. Même si le niveau de preuve scientifique n'est pas encore suffisant pour pouvoir proposer ce traitement en première intention sur cette base scientifique pour des métastases hépatiques hors cancers colorectaux ou tumeurs primitives hors carcinomes hépatocellulaires, il est suffisant pour pouvoir le proposer pour les carcinomes hépatocellulaires(1) ou les métastases hépatiques de cancers colorectaux(2) de moins de 3 cm de diamètre, son efficacité antitumorale étant voisine de celle des résections chirurgicales non anatomiques et avec des taux de morbidité et de mortalité très inférieurs.
Lorsque la masse tumorale hépatique a une position centrale, il existe un risque de plaie iatrogène des voies biliaires intrahépatiques centrales ou de la voie biliaire principale à son origine et/ou du tube digestif, induisant alors une morbidité sévère et pouvant faire récuser l’indication de thermoablation.
Ces tumeurs centrales se situent dans la partie postérieure du segment IV, dans la partie antérieure du segment I, ou dans la partie interne du segment V ou du segment III. En cas d’antécédent d’ablation chirurgicale d’un hémi foie, ce sont quasiment toutes les lésions se situant dans la région de la moitié inférieure de la tranche de section hépatique qui peuvent être considérées comme étant centrales.
On admet qu’il devient risqué de traiter par thermoablation une lésion se situant à moins de 10 mm de la structure anatomique à ne pas léser. En effet, on essaie d’obtenir en règle générale une marge de sécurité de quelques millimètres en périphérie de la lésion à traiter.
Si la zone de thermoablation prévue doit atteindre la structure anatomique à ne pas léser, il faut soit récuser le patient en lui proposant éventuellement un autre traitement local non chirurgical soit faire une thermoablation avec une méthode de protection.
Les traitements non chirurgicaux
Les autres traitements possibles non chirurgicaux sont l’alcoolisation percutanée pour les petits carcinomes hépato-cellulaires(3), la radiothérapie ou encore l’électroporation irréversible ou IRE(4).
Cette dernière méthode, proposée en première intention par certaines équipes pour le traitement percutané des tumeurs centrales hépatiques, est techniquement difficile à mettre en œuvre, coûteuse, avec des procédures longues. Elle peut induire des plaies thermiques à des structures anatomiques adjacentes du fait d’un effet thermique associé à l’électroporation elle-même.
De manière générale, des méthodes de protection digestive et biliaire ont été développées avec un niveau de preuve néanmoins assez faible et des études de cohortes exclusivement rétrospectives(5). Elles peuvent consister en une hydrodissection avec du liquide glacé ou du G30. Il a également été proposé pour protéger le tube digestif d’utiliser une dissection au CO2 ou encore des ballons d’interposition. La modification de la position du patient ou la traction sur l’aiguille de thermoablation, décrites et pouvant être efficaces pour les thermoablations rénales, sont peu efficaces pour la pathologie hépatique. Enfin, il a été envisagé pour protéger les voies biliaires centrales d’effectuer un refroidissement biliaire par voies transhépatique, transvésiculaire, endoscopique ou chirurgicale via une cholédochotomie. La méthode d’interposition la plus fiable semble à priori celle utilisant du gaz qui est le meilleur isolant thermique, avec néanmoins pour le CO2 un inconvénient majeur qui est sa vitesse de résorption importante, laissant aléatoire la présence d’une interposition gazeuse efficace tout au long de la procédure, en particulier si l’espace anatomique intéressé par cette dissection est fin et peu extensible. Pour les voies biliaires centrales, le refroidissement biliaire est généralement efficace mais nécessite une procédure associée qui peut être compliquée techniquement chez les patients ayant un arbre biliaire non dilaté et être potentiellement morbide.
En somme, il reste probablement un espace de progression pour le traitement percutané de ces tumeurs hépatiques hilaires. Conjointement à ce constat, on sait que l’air ambiant est le meilleur isolant thermique, le moins cher et le plus facile à mettre en œuvre, avec une faible vitesse de résorption. Si on utilise l’air ambiant pour effectuer des interpositions aériques percutanées, les risques potentiels sont des risques septiques et d’embolisation vasculaire.
Néanmoins, le risque septique paraît à priori faible, les procédures étant réalisées dans un contexte de bloc opératoire, avec des volumes d’air injecté très faibles. Le risque potentiel de complication clinique du fait d’une embolisation vasculaire paraît également faible pour les veines et quasi nul pour les artères du fait d’un volume injecté faible et de contrôles itératifs scanographiques nécessaires lors de cette injection.
Comment faire une thermoablation de tumeur hépatique centrale sur coussin d’air ?
La première étape de la prise en charge est la réunion de concertation pluridisciplinaire au cours de laquelle sont di cutées toutes les possibilités techniques pour le patient. Une thermoablation avec interposition aérique dans le pédicule hépatique peut être proposée si la zone de thermoablation prévue se situe à moins de 10 mm des structures anatomiques adjacentes, biliaires centrales ou digestives. La deuxième étape est constituée par la consultation préthérapeutique au cours de laquelle doivent être spécifiées la possibilité d’échec technique et la possibilité de complications de type perforation ou sténose d’organes adja- cents à la zone de thermoablation. La procédure thérapeutique est ensuite réalisée sous anesthésie générale et sous contrôle impératif scanographique. L’aide de l’échographie est précieuse pour le positionnement de l’aiguille ou des aiguilles permettant l’interposition gazeuse de l’aiguille ou sonde de thermoablation.
Avec cette technique, on peut utiliser indifféremment comme source d’énergie la radiofréquence, les micro-ondes ou la cryothérapie, avec une ou plusieurs sondes ou aiguilles (tableau).
Déroulé de la procédure
Le positionnement de la sonde ou de l’aiguille doit être effectué avant toute tentative de protection. Débute ensuite la manœuvre de dissection aérique dans le pédicule hépatique avec une ou plusieurs aiguilles 22 G de 15 à 20 cm de longueur et avec une seringue de 10 ml luerlock (figures 1-3). On repère la graisse se situant dans la partie haute du pédicule hépatique à proximité des structures vasculaires et biliaires, et on positionne cette aiguille de 22 G.
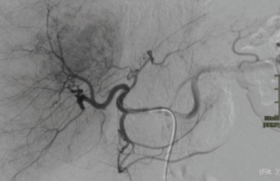
Figure 1. Reconstruction frontale scanographique après aérodissection dans le pédicule hépatique.
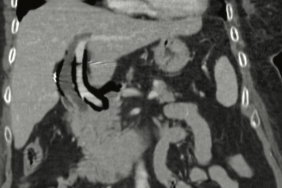
Figure 2. Aérodissection dans le pédicule hépatique avec sonde de micro-ondes en place dans la tumeur du segment hépatique IV bas (tête de flèche), aiguille 22 G d’interposition en place dans la graisse du hile hépatique (flèche) et avec migration d’air dans la partie non vascularisée du petit épiploon ou ligament gastro-hépatique (étoile).
Figure 3. Femme de 75 ans ayant eu il y a 5 ans une hépatectomie droite pour un carcinome hépatocellulaire et présentant une récidive tumorale de 18 mm de diamètre se situant dans le segment IV bas au contact du côlon et de la convergence biliaire primaire.
On effectue ensuite une injection test de 1 à 2 cm3 d’air ambiant et on repositionne l’aiguille tant que l’air ne migre pas dans l’espace anatomique voulu. Cette étape peut être très rapide mais reste la plus technique, pouvant nécessiter la mise en place de plusieurs aiguilles. Elle peut être également la plus dangereuse si on injecte sans contrôle plusieurs dizaines de cm3 d’air ambiant dans les systèmes veineux sus-hépatique ou portal. L’utilisation d’une seringue, et non d’un insufflateur, est très utile. Cela permet d’avoir la sensation de résistance à l’injection qui est une aide pour trouver l’espace anatomique, ayant en règle une résistance moindre à l’injection que le parenchyme hépatique.
Si c’est le pédicule hépatique qui est visé, la migration d’air se fait exclusivement dans le petit épiploon, silhouettant ainsi l’artère, la veine porte et la convergence biliaire primaire, ainsi que la voie biliaire principale, et sans migration d’air dans la grande cavité péritonéale. L’interposition aérique ne nécessite alors qu’une injection d’un faible volume d’air, de l’ordre de 20 à 30 cm3 en moyenne.
On peut voir ainsi progresser l’air vers la gauche dans le ligament gastrohépatique qui correspond à la partie non vascularisée du petit épiploon et vers le bas en périphérie du pédicule vasculaire mésentérique supérieur et/ou splénique (figures 1 et 2).
Un succès technique, autorisant la réalisation de la thermoablation, est obtenu lorsque l’on parvient à avoir un coussin d’air continu d’au moins 1 mm d’épaisseur autour de la structure à protéger ou en interposition avec la zone de thermoablation prévue. En cas de protection de la convergence biliaire primaire, il n’est pas possible d’avoir une dissection de plus de 2-3 mm, cette épaisseur étant néanmoins suffisante pour assurer l’isolation thermique.
L’injection d’air étant stable dans le temps, il n’est pas nécessaire le plus souvent de réinjecter de l’air au cours de la thermoablation, l’aiguille ou les aiguilles d’inter-position pouvant ainsi être ôtées avant le début de la thermoablation proprement dite.
Dans les cas où l’aiguille d’interposition gazeuse est laissée en place au cours de la thermoablation, du fait par exemple d’une très fine interposition gazeuse qui peut à tout moment ne plus suffire, il est important de la toucher régulièrement afin de dépister rapidement une éventuelle migration thermique le long de l’aiguille qui peut occasionner, si elle existe, une brûlure cutanée au point de ponction de l’aiguille d’interposition.
La fin de la procédure se déroule comme une procédure de thermoablation percutanée standard.
En cas de migration d’air perprocédure dans le système veineux portal, il n’est pas nécessaire d’entreprendre une anticoagulation post-opératoire pour prévenir une éventuelle thrombose cruorique.
Enfin, du fait d’un risque septique potentiel en utilisant l’air ambiant, il peut exister un rationnel pour administrer une anti-bioprophylaxie pendant 48 heures.
Le suivi évolutif clinique en imagerie est également standard avec un contrôle en imagerie (plutôt en IRM) 4 à 6 semaines après la procédure thérapeutique. Il n’est pas nécessaire de prévoir un contrôle plus rapproché à la recherche systématique d’une complication post-thérapeutique.
Quels résultats espérer en cas de thermoablation de tumeur centrale hépatique sur coussin d’air ?
Nous avons débuté il y a quelques années cette technique et avons communiqué des résultats préliminaires et originaux lors du dernier congrès de l’ECIO(6). Cette étude rétrospective préliminaire a été réalisée sur 60 patients consécutifs de notre centre entre 2013 et 2021, parmi 1 318 patients ayant eu une thermoablation hépatique au cours de cette période.
Ces patients avaient une lésion hépatique unique de 24,8 ± 12 mm, centrale, avec contact potentiel de la zone de thermoablation par les voies biliaires centrales (41,7 %) et/ou le tube digestif (61,6 %) et une protection dans le pédicule hépatique, associée éventuellement à un protection interhépato-digestive et à l’air ambiant.
Les patients ont été traités en majorité pour un carcinome hépatocellulaire (60,0 %) ou des métastases de cancer colorectal (26,7 %) et en utilisant une seule sonde de micro-ondes pour tous les patients (Amica).
Les positionnements des aiguilles d’interposition et de la sonde de micro-ondes ont été réalisés sous anesthésie générale et contrôle mixte échographique et scanographique avec injection iodée intraveineuse, selon la technique décrite précédemment.
Un succès technique était obtenu dans 85,0 % des cas, le plus souvent avec une seule aiguille d’interposition (93,3 %). Le temps de procédure total était de 45,2 ± 18,0 minutes.
Aucune complication peropératoire n’a été rapportée. Des complications précoces étaient observées dans 16,7 % des cas avec 15,0 % de complications mineures correspondant le plus souvent à des douleurs modérées, accessibles à des antalgiques de niveau 1, et une complication majeure correspondant à une pneumopathie d’inhalation. Aucune infection hépatobiliaire ni complication ischémique n’ont été observées.
La durée d’hospitalisation moyenne était de 2,7 jours. Des complications tardives étaient présentes dans 8,3 % des cas, toutes mineures et correspondant à une dilatation de canaux biliaires sous-segmentaires, au contact de la zone de thermoablation, non symptomatique et ne nécessitant aucun traitement.
À 3 mois, une réponse complète tumorale selon les critères de RECIST modifiés était notée dans 86,2 % des cas. Au cours d’un suivi évolutif médian de 18,8 mois, une récidive locale était observée dans 40,0 % des cas et une récidive à distance dans 58,6 % des cas. La survie moyenne sans récidive locale était de 12,1 mois et la survie moyenne sans récidive tumorale à distance était de 11,1 mois.
Les résultats de cette étude rétrospective et monocentrique semblent donc indiquer que l’interposition gazeuse à l’air ambiant pour des tumeurs hépatiques centrales peut être pratiquée dans la majorité des cas, avec un temps de procédure court, sans augmenter la morbidité de la procédure ni son coût et avec un contrôle tumoral paraissant similaire à celui obtenu pour des tumeurs hépatiques périphériques.
Il faudra bien sûr les confirmer par des études prospectives pratiquées dans de multiples centres, et les comparer de manière randomisée à la technique la plus concurrentielle actuellement qui est l’électroporation irréversible et à une technique similaire à celle décrite dans cet article mais utilisant le CO2 comme gaz isolant.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :