Grand angle
Publié le 29 juin 2022Lecture 15 min
Techniques de protection en thermoablation
Pierre-Alexis AUTRUSSEAU, Pierre AULOGE, Guillaume KOCH, Roberto Luigi CAZZATO, Afshin GANGI, Julien GARNON, Service d’imagerie interventionnelle, Nouvel hôpital civil, Strasbourg
Les ablations thermiques sont un traitement efficace dans de nombreux organes pour des tumeurs malignes ou bénignes. Bien que leur abord soit mini-invasif, le risque de lésion non désirée d’un organe adjacent est réel avec de multiples cas de lésions thermiques aux conséquences graves rapportées dans la littérature. La mise en œuvre des techniques de protection a un double objectif : prévenir les lésions thermiques des organes adjacents et permettre de faire des ablations plus agressives afin d’améliorer le contrôle local. L’objectif de cet article est de décrire les principales modalités de protection et leurs applications.
Techniques de dissection
Les techniques de dissection consistent à injecter un agent liquide ou gazeux de manière percutanée. Il s’agit de techniques bon marché et relativement simples à mettre en œuvre sous réserve d’une bonne connaissance des espaces anatomiques afin que la protection soit efficace et optimale.
Hydrodissection
L’hydrodissection consiste à injecter du liquide (sérum physiologique ou glucosé) dans un espace anatomique. Elle est réalisable pour tout type d’ablation (par le chaud ou par le froid) et dans n’importe quelle localisation. L’objectif est à la fois de créer une distance de sécurité entre la tumeur à traiter et l’organe à risque, mais également de permettre un effet de dissipation thermique en maintenant un flux d’injection lors de l’ablation. Ce dernier point est particulièrement important lorsque la distance de sécurité créée n’excède pas quelques millimètres (espace épidural, par exemple) ou en tout cas pas le centimètre. Un thermomètre placé à l’interface tumeur – organe vulnérable peut être combiné à l’hydrodissection lors des cas à risque, ce afin d’adapter le débit d’injection lors de la phase d’ablation.
Techniquement, une aiguille spinale de faible calibre (18G, 20G ou 22G) est insérée sous contrôle d’imagerie entre la lésion à traiter et l’organe à protéger, idéalement au niveau d’une interface graisseuse qui représente une cible idéale pour la pointe de l’aiguille. Une faible quantité de liquide de dissection (5 à 10 mL) permet de tester et vérifier la distribution satisfaisante du produit, ou alors la nécessité de repositionner la pointe de l’aiguille. Puis, des volumes plus larges (de quelques dizaines de millilitres à 1-2 litres) peuvent être injectés jusqu’à obtenir un déplacement satisfaisant de l’organe. Plusieurs aiguilles sont parfois nécessaires pour éloigner la totalité d’un organe de la lésion.
Le liquide injecté peut être soit du sérum physiologique soit du sérum glucosé.
Ce dernier doit être utilisé en association à la radiofréquence afin d’éviter la conductivité électrique par les ions. Pour les autres modalités d’ablation, les deux types de sérum sont utilisables. Le liquide peut être injecté à température ambiante (autour de 20 °C) pour les ablations thermiques par le chaud, ou alors à température plus élevée (autour de 37 °C) pour les ablations par le froid. En scanner, sa visibilité est améliorée par un mélange de produit de contraste iodé de faible osmolalité (Visipaque® 270 ; General Electric, États-Unis) dilué à 5 % (1/20). Seule la dissection au niveau de l’espace épidural nécessite une concentration de contraste plus importante (50 %) pour permettre une identification certaine de l’espace de diffusion du liquide. La qualité de la dilution dans la seringue est vérifiée en scanner avant injection, afin de ne pas gêner le reste de l’intervention en cas d’une densité de contraste trop élevée.
L’hydrodissection est possible en sécurité avec de larges volumes (> 1 litre) dans les espaces sous-cutanés, le péritoine, le rétro-péritoine, le médiastin ou l’espace épidural sans entraîner de phénomène compressif. La raison est la diffusion du liquide dans d’autres espaces anatomiques (par exemple, du péritoine vers la plèvre au travers des puits de Ranvier ; de l’espace épidural thoracique vers la plèvre au travers des foramens intervertébraux, etc.) et sa réabsorption rapide par les séreuses. L’injection de très larges volumes de liquide (> 3 litres dans la littérature) doit être évitée en raison du risque de déséquilibre hydro-électrolytique.
Au total, l'hydrodissection est un technique fiable, facile d'accès, peu chère. Les principales causes d'échec sont les adhérences post-opératoires (l'ascite artificielle a, par exemple, peu de chance de fonctionner après chirurgie hépatique) ou post-radiothérapie. Les différentes études n'ont pas rapporté de diminution du contrôle local lors de l'utilisation de l'hydrodissection en ablation.
• Cas pratique en thermo-ablation hépatique : ascite artificielle (figure 1)
Le foie présente une anatomie complexe, avec toute une face péritonéalisée. Les séreuses sont un espace anatomique où peut être aisément diffusé du liquide de dissection. Une des applications reconnues est la réalisation d’une ascite artificielle à visée de protection thermique du diaphragme lors des ablations de tumeurs sous-capsulaires au contact du diaphragme, notamment dans les segments VII et VIII.
Technique : sous échographie, une aiguille spinale 20G est utilisée pour ponctionner la partie basse du segment VI avec un trajet ascendant. Un microguide 0,018 est inséré dans l’aiguille 20G, qui va initialement avancer dans le parenchyme hépatique. Le microguide est rentré à l’intérieur de l’aiguille, qui est elle-même délicatement reculée et verticalisée, permettant le passage du guide dans le péritoine en direction du dôme hépatique. La trajectoire du microguide doit être vérifiée par scanner ou sous fluoroscopie. En effet, une ponction trop haute pourra faire avancer le microguide dans l’espace pleural plutôt que dans l’espace péritonéal. Un cathéter 6 French est monté en co-axial sur le guide, puis un mélange de 50 mL de liquide d’hydrodissection est injecté pour vérifier la bonne diffusion intrapéritonéale. En cas de bon positionnement, l’injection de 500 mL du mélange permet de décoller le foie du diaphragme et de la paroi abdominale. Lors de l’ablation, une injection continue à environ 0,5 mL/sec permet de maintenir un flux refroidissant le diaphragme ou la paroi abdominale. Le volume injecté total est d’environ 800 mL à 1 L. En plus de prévenir les lésions diaphragmatiques, l’ascite artificielle est aussi responsable de moins de douleurs postopératoires. La protection de la paroi abdominale lors des thermoablations des tumeurs des segments V et VI est également une bonne indication.
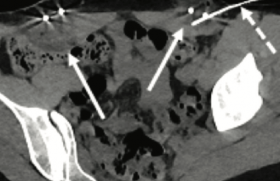
• Cas pratique en thermo-ablation rachidienne : hydrodissection épidurale (figure 2)
Les ablations rachidiennes sont souvent considérées à risque en raison de la présence des nerfs rachidiens ou du cordon médullaire. De plus, il s’agit d’un espace osseux clos où les structures ne pourront être déplacées uniquement de quelques millimètres, et où l’objectif sera de maintenir un flux continu d’injection afin de dissiper l’énergie thermique.
Technique : une aiguille spinale 18G est insérée sous contrôle scanographique dans l’espace épidural par voie interlamaire au plus proche de la lésion à traiter. Le liquide d’hydrodissection permet de confirmer la bonne répartition épidurale et repousse légèrement le fourreau dural. Le déplacement est plus important en lombaire où le cordon médullaire est déjà terminé. L’excès de liquide injecté ressort par les foramens vertébraux dans le rétropéritoine ou dans la plèvre selon l’étage. Un thermomètre à bout mousse peut être utilisé en co-axial dans l’aiguille d’hydrodissection à l’aide d’un Y à valve afin de vérifier l’efficacité de la dissection (diminution de la température au contact de la tumeur lors de l’injection du liquide) et de monitorer l’ablation. L’injection est maintenue lors de l’ablation de manière lente mais régulière (0,5 mL/sec) et adaptée à la température sur le thermomètre afin de n’injecter que le volume nécessaire. Les causes d’échec peuvent être les antécédents de radiothérapie, les adhérences sur tumeurs inflammatoires ou sur une épidurite tumorale.
Carbodissection
L’injection de liquide d’hydrodissection à tendance à diffuser en déclive en raison de la gravité dans les cavités anatomiques (plèvre, péritoine). L’alternative à l’injection d’un liquide d’hydrodissection est l’injection de gaz, qui aura lui tendance à se distribuer vers le haut. L’air ambiant ne doit plus être utilisé en raison du risque d’embolie gazeuse, et, à l’opposé, le CO2 médical à moins de risque d’entraîner une embolie gazeuse symptomatique. En ablation thermique, la carbodissection permet non seulement de déplacer physiquement les organes environnants mais aussi de réaliser une isolation thermique en ne conduisant pas l’énergie de la modalité d’ablation. L’efficacité de l’isolation thermique du CO2 est même supérieure à celle de l’air. Le recul sur cette technique est important puisqu’elle est largement utilisée en chirurgie lors des laparoscopies ou thoracoscopies.
Techniquement, le matériel utilisé est le même que pour une angiographie au CO2. Une aiguille de petit calibre est insérée à l’endroit où le CO2 doit être injecté. Des aiguilles à bout mousse avec une pointe sur ressort peuvent être utilisées pour pénétrer la plèvre ou le péritoine sans lésion pulmonaire ou du tube digestif. Une petite quantité de CO2 est injectée (50 mL) afin de vérifier le bon positionnement. En cas de distribution satisfaisante, de plus grandes quantités peuvent être injectées (1,5 L). Il faut prêter une attention particulière à l’absorption du CO2 par les séreuses, qui nécessite de surveiller pendant l’ablation que le CO2 est encore présent en quantité 2 suffisante et, le cas échéant, maintenir une injection régulière.
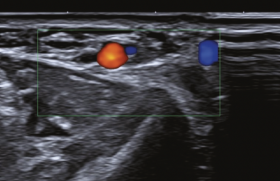
• En pratique : pneumothorax externe au CO2 (figure 3)
Lors des ablations pulmonaires proches des parois ou des ablations pariétales thoraciques, il peut être judicieux de réaliser un pneumothorax externe au CO2 à visée de protection.
Technique : une aiguille à bout mousse montée sur ressort 17G (Hydroguard® ; AprioMed, Suède) est amenée sous contrôle scanographique au contact de la plèvre, qui est ponctionnée jusqu’à ce que le ressort lâche. L’aiguille peut être avancée librement avec le bout mousse dans la cavité pleurale sans résistance. En imagerie, l’aspect est trompeur avec une image évocatrice de l’aiguille au sein du parenchyme pulmonaire. Une petite quantité de CO2 (50 mL) est injectée et réalise une lame de pneumothorax. En cas de distribution satisfaisante, une plus large quantité peut être injectée jusqu’au décollement du poumon en regard de la zone d’ablation. La plèvre réabsorbant rapidement le CO2, l’injection doit être régulière au cours du geste. En fin d’intervention, le CO2 restant peut être reaspiré au travers de l’aiguille afin de réexpandre le poumon. En l’absence de brèche pulmonaire, un drainage externe ne sera normalement pas nécessaire mais peut être laissé par précaution pour 24 heures.
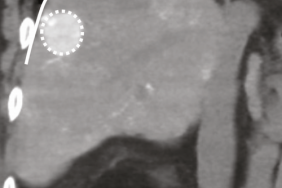
• En pratique : pneumopéritoine externe au CO2 (figure 4)
Les ablations de paroi abdominales, surtout chez les patients minces, peuvent se révéler compliqués en raison de la présence du tube digestif à proximité immédiate de la zone d’ablation. Le pneumopéritoine, grâce à la distribution vers le haut du CO2, va permettre d’éloigner le tube digestif de la paroi abdominale.
Technique : de la même manière que pour la plèvre, une aiguille à bout mousse montée sur ressort 17G (Hydroguard® ; Aprio-Med, Suède) est amenée sous contrôle scanographique au contact du péritoine. La ponction se fait également jusqu’au relâchement du ressort. Une petite quantité de CO2 est injectée (50 mL), puis une plus grande en cas de répartition satisfaisante. Dans tous les cas, le pneumopéritoine au CO2 doit être réalisé sous supervision anesthésiologique en raison de modifications hémodynamiques liées à l’augmentation de la pression intra-abdominale, pouvant avoir des conséquences cardiovasculaires mais aussi de perfusion d’organe.
Hémodissection
Un des inconvénients majeurs de l’hydrodissection et de la carbodissection est la réabsorption rapide après injection et sa diffusion hors du site d’injection, entraînant un risque de lésion en cas de manque de surveillance lors de l’ablation. L’injection de caillot autologue permet une moindre diffusion en raison de sa viscosité plus élevée, ainsi qu’une durée de présence accrue lors du caillotage. Il s’agit d’une technique simi-aire à celle du blood-patch. Cette technique n’a été que très peu décrite dans la littérature.
• En pratique : hémodissection de l’espace interprostatorectal
Dans le cas des cryoablations prostatiques, le rectum qui est à proximité immédiate de la prostate doit être protégé. Une aiguille de plus gros calibre qu’habituel, montée sur un cathéter 5 French, est insérée par voie transpérinéale sous contrôle échographique à l’aide d’une sonde endo-rectale. L’utilisation d’une sonde endo-rectale avec une barrette linéaire supplémentaire facilite la mise en place de l’aiguille de dissection. Ainsi, 5 mL de sérum salé physiologique est injecté afin de vérifier la bonne diffusion dans l’espace interprostatorectal. Puis, un volume de 40 mL de sang est prélevé stérilement au patient, puis injecté au travers du cathéter 5 Fr jusqu’à une bonne séparation de la prostate et du rectum.
Techniques de déplacement physique
Interposition de ballons (figure 5)
En cas d’échec des techniques précédentes, l’insertion co-axiale d’un ou plusieurs ballons d’angioplastie montés sur guide peut être essayée. Le ballon permet à la fois un déplacement physique des structures lors de son inflation, et l’utilisation de gaz pour le remplir (air ou CO2), soit une isolation thermique. La principale limite est le positionnement difficile des ballons, qui ont tendance à glisser, reculer et dont l’avancement peut être compliqué. L’interposition de ballons a été rapportée comme efficace, y compris en cas d’adhérences post-opératoires.
Déplacement mécanique par des aiguilles à bout mousse
Les aiguilles à bout mousse atraumatiques peuvent permettre, seules ou en complément d’une hydrodissection, de déplacer des structures mobiles notamment en intra-abdominal.
• En pratique : déplacement mécanique de l’estomac
Lors des ablations hépatiques des segments II et III, le lobe gauche du foie et l’estomac sont reliés notamment par le ligament hépatogastrique. L’hydrodissection n’est pas efficace, à moins de réussir à ponctionner directement le ligament pour que le liquide injecté reste en place et sépare physiquement le foie de l’estomac. Dans ce cas, deux aiguilles à bout mousse (Hydroguard® ou Softguard® ; AprioMed, Suède) 17G peuvent être insérées entre le foie et l’estomac, et un déplacement mécanique externe permettra de repousser l’estomac lors de l’ablation.
• En pratique : déplacement mécanique du côlon (figure 6)
Le constat est le même chez certains patients pour séparer le côlon du segment VI hépatique, siège d’un ligament hépato-colique inconstant. L’injection de liquide à ce niveau à tendance à fuser en intrapéritonéal comme pour une ascite artificielle et ne pas séparer physiquement le côlon du foie. Une des possibilités est de glisser une ou plusieurs aiguilles à bout mousse 17G (Hydroguard® ou Softguard® ; AprioMed, Suède) entre les deux structures, puis de réaliser un déplacement mécanique externe de l’aiguille afin de répercuter ce mouvement à l’intérieur de l’abdomen. L’aiguille est ensuite immobilisée à l’extérieur du patient, par exemple à l’aide d’un scratch, afin de garder le bénéfice du déplacement lors de l’ablation.
Traction des aiguilles
Lors d’une cryoablation, une des possibilités est de tracter manuellement la partie externe des aiguilles afin de déplacer la lésion traitée en interne, et ce après la réalisation d’un « stick » ou au début de l’ablation. Cette possibilité existe également lors d’une ablation par radiofréquence avec une électrode « parapluie ». En micro-ondes ou radiofréquence avec une aiguille droite, la traction n’est pas possible car la lésion n’est pas fixée, un mouvement de levier reste toutefois possible.
L’organe le plus facile à déplacer reste le poumon, notamment grâce à sa grande compliance. Cette technique est également possible dans le rein ou le foie, mais avec un déplacement beaucoup plus limité en raison de la moins grande compliance des organes.
• En pratique : traction d’un nodule pulmonaire en cryoablation (figure 7)
Le nodule pulmonaire est ponctionné à l’aide d’une ou plusieurs cryoablations selon la planification préétablie. Une cryoadhésion (stick) est lancée sur les aiguilles. Au bout de 30 secondes, une traction douce est réalisée sur les aiguilles permettant un déplacement du nodule sur plusieurs centimètres. Une pince plastique mise à la peau permet de maintenir cette traction lors de l’ablation. Ce déplacement permet d’éloigner le nodule d’une structure où l’ablation n’est pas désirée, comme le diaphragme. Cette traction peut être également responsable d’une lame de décollement, améliorant l’effet d’insulation thermique. Lors de la décongélation passive puis active, le nodule peut se remettre à sa position d’origine. Dans ce cas-là, un stick peut être maintenu à tour de rôle sur chaque aiguille de cryoablation afin de ne pas perdre le bénéfice de la traction.
Perfusion endoluminale
Le principe de la perfusion endoluminale est l’injection d’un liquide chaud (37 °C) ou à température ambiante (20 °C) en fonction de la modalité d’ablation au sein d’un organe creux afin de protéger sa paroi et de limiter le risque de perforation. En théorie, n’importe quel organe creux pourrait bénéficier de cette technique. En pratique, elle est principalement limitée aux voies biliaires ou aux voies urinaires.
• Perfusion biliaire
L’objectif est d’injecter du liquide (sérum salé physiologique ou sérum glucosé à 5 % selon la modalité d’ablation) au sein des voies biliaires afin de les protéger d’une lésion thermique qui serait responsable d’une sténose biliaire retardée. Ces lésions sont d’autant plus graves qu’elles sont proximales ou sur la bifurcation biliaire.
Deux possibilités pour cathétériser les voies biliaires. La première consiste à la mise en place endoscopique d’un cathéter naso-biliaire de 5 Fr, positionné au contact de la tumeur à traiter. La seconde possibilité est la ponction directe à l’aiguille spinale des voies biliaires, d’autant plus difficile que ces voies ne sont pas dilatées. Du liquide est ensuite perfusé à un débit d’environ 1- 2 mL/sec lors de l’ablation. Cette technique, tout comme l’hydrodissection, ne diminuerait pas le contrôle local après traitement. Elle est aujourd’hui peu utilisée en pratique car complexe à mettre en œuvre et en raison de la possibilité de limiter les risques de lésion biliaire en utilisant l’électroporation irréversible. Un exemple est fourni avec la figure 8.
Perfusion urétérale
Les ablations thermiques proches de l’uretère ou de la jonction pyélo-urétérale sont à risque, tout comme l’arbre biliaire, de sténoses retardées. Cette technique peut être mise en place lorsque l’hydrodissection de la jonction pyélo-urétérale ou de l’uretère ne permet pas un déplacement suffisant. La pyéloperfusion rétrograde consiste à la mise en place d’une sonde urétérale 6 Fr par les voies naturelles avant l’ablation, permettant un accès afin de perfuser du sérum salé ou glucosé à l’aide d’une poche à une pression de 80 cm d’eau. Une sonde urinaire est mise en place en parallèle pour évacuer le liquide injecté. Cette voie d’abord est préférée pour les ablations proches de la jonction pyélo-urétérale, car la sonde ne tient pas correctement en place pour les ablations à proximité de l’uretère. À la fin du traitement, la sonde peut être retirée ou remplacée par une sonde JJ pour les 6 à 9 semaines suivantes si le risque de sténose post-opératoire est élevé.
La pyéloperfusion antérograde consiste à ponctionner les cavités urinaires par voie percutanée à l’aide d’une aiguille 20G, à cathétériser les voies urinaires à l’aide d’une guide 0,018 puis à monter un cathéter 5 Fr. Ce cathéter doit être mis en place au plus proche de la zone d’ablation, c’est-à-dire dans le pyélon pour l’ablation d’une tumeur centrale du rein ou dans l’uretère pour l’ablation d’une tumeur rétro-péritonéale à proximité de l’uretère. De la même manière que pour les voies biliaires, cette façon de procéder peut s’avérer plus compliquée si l’arbre urinaire n’est pas dilaté. Ensuite, du sérum physiologique ou glucosé (selon la modalité d’ablation) réchauffé ou à température ambiante est instillé à un débit d’environ 1- 2 mL/sec. Comme pour la pyéloperfusion rétrograde, une sonde urinaire est mise en place afin d’évacuer l’excès de liquide injecté. Comme les techniques précédentes, la pyéloperfusion n’aurait pas d’impact négatif sur le contrôle local des tumeurs traitées à proximité.
Techniques externes
Déplacement externe
Une dernière possibilité est d’utiliser une compression externe afin de déplacer des organes. Lors des ablations ou biopsies intra-abdominales, le tube digestif peut s’interposer entre la peau et la zone de traitement. L’appui avec la sonde d’échographie ou avec un poids peut permettre de déplacer le tube digestif à distance de la zone de traitement. Une attention particulière doit être amenée à ne pas traverser une anse digestive collabée par la pression. De plus, cette technique peut être utilisée pour la cryoablation en raison de la visualisation de la glace, mais la séparation/l’efficacité est beaucoup plus difficile à évaluer pour les ablations thermiques par le chaud où les limites de la zone d’ablation ne sont pas connues. De plus, la pression doit être continue tout au long de la biopsie ou du traitement, afin de ne pas permettre de mouvement des structures au relâchement.
Réchauffement cutané
Les cryoablations percutanées des volumineuses tumeurs des tissus mous, comme les tumeurs desmoïdes, peuvent être à risque de nécrose cutanée. Ces tumeurs, sièges d’une vasoconstriction lors du second cycle de cryoablation, mettent beaucoup de temps à se réchauffer et à faire fondre le glaçon. Une attention particulière doit être portée au positionnement du patient dans son lit à la sortie de l’intervention. Pour une tumeur dorsale, le repositionnement en décubitus dorsal peut mettre en contact la tumeur qui est encore gelée et la peau, à risque important de complication cutanée par la suite. Une simple vessie chaude ou des gants avec un liquide chaud à l’intérieur peuvent permettre un réchauffement cutané et d’éviter ces complications.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :