Publié le 28 mar 2023Lecture 3 min
Chimio-Lipiodol® intra-artérielle hépatique sans embolisation dans le carcinome hépatocellulaire - Essai de phase II multicentrique LIDA-B II
Chloé GUILLOT, Boris GUIU, service de radiologie diagnostique & interventionnelle, hôpital Saint-Eloi, CHU de Montpellier
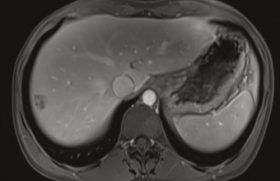
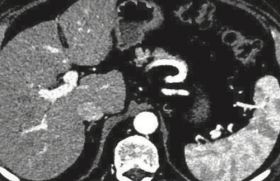
Le traitement optimal des patients atteints d’un carcinome hépatocellulaire (CHC) non métastatique non résécable avec une fonction hépatique préservée Child-Pugh A ou B7(1), reste à déterminer. Dans la mesure où elle augmente la survie des patients(2-5), la chimioembolisation (CHE) ou chimiothérapie intra-artérielle (CIA), suivie d’une embolisation des artères nourricières de la(des) tumeur(s) est considérée par les groupes d’experts comme le traitement de référence du CHC de stade intermédiaire B de la classification de Barcelone.
Rationnel
Il apparaît toutefois que la chimiothérapie intra-artérielle hépatique (CIAH) est « logique » pour le traitement des CHC. En effet, les CHC sont vascularisés par le système artériel hépatique et non par le système veineux porte, contrairement au parenchyme hépatique non tumoral(6). Une perfusion intra-artérielle hépatique de certains agents anticancéreux, dont les anthracyclines, aboutit à une forte extraction par le foie dès le premier passage, une importante concentration intratumorale et une concentration systémique basse(7-8). De plus, l’absence d’embolisation, à la différence donc d’une CHE, permet de limiter considérablement la toxicité du traitement.
L’émulsion idarubicine-Lipiodol®
Dans le cadre de l’essai clinique LIDA-B II, l’idarubicine a été choisi suite à l’étude pharmacologique préclinique in vitro(9-10). En effet, il ressort que l’idarubicine, molécule de la famille des anthracyclines, est l’agent anticancéreux le plus cytotoxique in vitro sur trois lignées de cellules de CHC. L’étude de phase I, LIDA-B, a permis d’évaluer la dose maximale tolérée à 20 mg par cure(11).
Lorsqu’il est injecté dans l’artère hépatique, le Lipiodol® à la propriété de se maintenir au contact du tissu tumoral et péritumoral hépatique (qu’il s’agisse d’un CHC ou d’une métastase) plusieurs semaines, voire plusieurs mois, alors qu’il est éliminé du parenchyme hépatique sain dans les 7 jours suivant son injection(12-14). Depuis les années 1980, il a prouvé son intérêt en termes de vecteur pour différents agents anticancéreux dans les traitements intra-artériels du CHC.
Il a été démontré que l’émulsion idarubicine-Lipiodol® est plus stable que l’émulsion doxorubicine-Lipiodol® en raison de la lipophile supérieure de l’idarubicine(15). Cette émulsion plus stable se traduit par une amélioration du profil pharmacocinétique de la drogue avec moins de passage systémique. Ces résultats sont confirmés dans l’étude de phase I LIDA-B avec un bénéfice net en termes de pharmacocinétique pour l’émulsion idarubicine-Lipiodol® par rapport à l’injection veineuse d’idarubicine.
Figure. Représentation schématique de l’essai clinique LIDA-B II.
Essai clinique
L’essai clinique de phase II piloté par le CHU de Montpellier, LIDA-B II, a débuté en mai 2018. Cette étude interventionnelle, prospective, monobras, multicentrique (6 centres participants dans toute la France), a prévu d’inclure 53 patients atteints de CHC non résécable, non métastatique sur cirrhose Child A/B7. Le nombre de sujet nécessaire a été estimé en considérant une puissance statistique de 90 %, un risque unilatéral à 0,05, pas d’analyse intermédiaire et 5 % de patients perdus de vue.
Les patients seront traités par 4 cures de chimiothérapie intra-artérielles hépatique, dont chacune consiste à l’injection en foie total d’une émulsion composée de 20 mg d’idarubicine (Zavedos®, Pfizer) diluée dans 5 ml d’eau ppi mélangée à 10 ml de Lipiodol® (Lipiodol Ultra-Fluide®, Guerbet) à l’aide d’un système de mélange et d’injection (Vectorio®, CE 0459, Guerbet) permettant le mélange et l’administration simultanée de Lipiodol® et d’un anticancéreux. Les cures sont réalisées toutes les 3 semaines.
L’objectif principal de l’étude est le taux de contrôle de la maladie (réponse complète, partielle ou stabilisation) à 4 mois de la première cure, selon les critères RECIST modifiés (encadré).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :