Kezaco
Publié le 10 juil 2023Lecture 9 min
Apport de la radiologie interventionnelle en contexte de soins palliatifs
Arthur DAVID1, Christophe PERRET2, Frédéric DOUANE1, Diane CONSTANT-DAVID3*

La radiologie interventionnelle (RI) a un rôle important dans la prise en charge des patients atteints de cancer, du diagnostic (biopsies) à la thérapeutique (thermoablation, chimioembolisation, radioembolisation, etc.) et maintenant également dans le traitement palliatif des symptômes liés au cancer. L’évolution constante des techniques a ainsi permis d’élargir le rôle du radiologue interventionnel au sein des équipes multidisciplinaires confrontées à des symptômes retentissant sur le confort des patients, en proposant des interventions efficaces avec une morbidité minimale, dans le but d’améliorer leur qualité et leur confort de vie.
En quoi consistent les soins palliatifs ?
L’Organisation Mondiale de la santé définit les soins palliatifs comme « une approche permettant d’améliorer la qualité de vie des patients et de leur famille, confrontés aux problèmes liés à des maladies potentiellement mortelles. Ils préviennent et soulagent les souffrances grâce à la reconnaissance précoce, l’évaluation correcte et le traitement de la douleur et des autres problèmes (physiques, psychosociaux ou spirituels) »(1). Il s’agit donc d’une prise en charge globale, nécessitant une collaboration multidisciplinaire des personnels médicaux, paramédicaux, des assistantes sociales, des psychologues, des diététiciens, etc. Ce travail d’équipe a pour objectif d’aider les patients et leur famille à vivre le mieux possible dans un contexte de maladie sévère, voire potentiellement mortelle, à travers une prise en charge experte des symptômes, un soutien psychosocial, ainsi qu’une aide à la décision vis-à-vis des traitements proposés, en fonction de la balance bénéfice/risque et du pronostic de la maladie. Les soins palliatifs ne doivent pas être réservés aux stades très tardifs d’une maladie grave, quand toutes les thérapeutiques curatives ont été épuisées. Au contraire, il est important d’intégrer l’identification et le soulagement des symptômes le plus tôt possible dans la prise en charge des patients, ce qui permet d’améliorer leur qualité de vie et celle de leurs proches, de réduire la médicalisation de la fin de vie, voire d’allonger la durée de vie (par une meilleure tolérance aux traitements curatifs)(2,3).
Figure 1. Illustration des deux types d’approches pour la mise en place des soins palliatifs après annonce du diagnostic de maladie incurable. En haut, l’approche tardive avec mise en place des soins palliatifs en vue d’accompagner la fin de vie après la fin des thérapeutiques actives. En bas, l’approche précoce, avec soins palliatifs déployés en parallèle des thérapeutiques actives, dans le but d’améliorer la qualité de vie des patients à tous les stades de la maladie (d’après [2,3]).
Apports de la RI en soins palliatifs
Les procédures de RI peuvent tout à fait être adaptées au contexte palliatif dans la mesure où elles offrent la possibilité de soulager un certain nombre de symptômes avec des risques plus faibles que d’autres alternatives, notamment chirurgicales (tableau).
Gestion de la douleur
De multiples techniques de RI existent pour proposer une solution antalgique au patient atteint de lésions néoplasiques douloureuses. Une analyse multidisciplinaire du dossier est nécessaire pour identifier le mécanisme lésionnel en cause dans le tableau douloureux, afin de proposer l’intervention la plus adaptée, voire une combinaison d’interventions en cas de mécanismes multiples.
• Neurolyse percutanée
La neurolyse percutanée est un traitement efficace des douleurs réfractaires en contexte néoplasique, en particulier pour les douleurs viscérales relayées par le système sympathique. Ainsi, différents relais peuvent être ciblés, parmi lesquels le ganglion stellaire (douleurs post-mastectomie, douleurs par envahissement direct des tumeurs de la tête et du cou), les plexus cœliaques/splanchniques (douleurs liées aux tumeurs abdominales notamment pancréatiques, figure 2), les plexus hypogastriques (douleurs viscérales pelviennes) ou le ganglion impar (douleurs périnéales)(4). La neurolyse percutanée est généralement réalisée sous anesthésie locale ou sédation consciente, avec guidage échographique ou scanographique en fonction de la localisation. La destruction nerveuse est réalisée à l’aide d’agents chimiques (éthanol absolu ou phénol 5 % ou 10 %) ou thermique (radiofréquence, cryothérapie, micro-ondes).
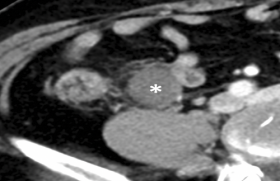
Figure 2. Neurolyse : exemple d’un patient présentant des douleurs abdominales réfractaires en lien avec un adénocarcinome pancréatique localement avancé. Hélice scanographique avec injection de produit de contraste par l’aiguille fine pour confirmer la bonne position avant alcoolisation du plexus cœliaque.
• Traitement des douleurs liées aux métastases osseuses : cimentoplastie, thermoablation, embolisation
Même si la radiothérapie externe reste un traitement de référence chez les patients présentant des douleurs liées à des métastases osseuses, son efficacité n’est pas systématique et survient souvent après un délai de plusieurs semaines. Les techniques de RI peuvent donc être proposées en alternative ou en combinaison avec la radiothérapie. On distingue classiquement les techniques ablatives, visant à obtenir une destruction tumorale (thermoablation, embolisation) des techniques de consolidation, dont l’objectif est de stabiliser les foyers de fractures (cimentoplastie, ostéosynthèse percutanée)(5).
La thermoablation correspond à la destruction thermique de tissu tumoral par une élévation (au-dessus de 60 °C, par radiofréquence ou micro-ondes) ou un abaissement (en-dessous de – 40 °C, par cryothérapie) de la température intratumorale. Dans le contexte de métastase osseuse douloureuse, elle permet un effet antalgique par destruction de l’interface tumeur-périoste, décompression tumorale, inhibition de l’activité ostéoclasique et diminution du relargage tumoral de cytokines. La thermoablation est effectuée sous anesthésie générale, sous guidage échographique, scanner, IRM ou CBCT. Elle peut également être employée dans les maladies mono- ou oligo-métastatiques, à but curatif.
L’embolisation artérielle de métastases osseuses, initialement développée pour la réduction des risques de saignements peropératoires, est désormais également effectuée à but antalgique, en particulier dans les lésions hypervasculaires (métastases de néoplasies rénales, thyroïdiennes, de mélanome, de tumeur neuroendocrines, etc.). Elle est par exemple indiquée en cas d’échec des thérapeutiques classiques (notamment la radiothérapie), ou alors combinée ou en alternative aux autres méthodes de RI (cimentoplastie, thermoablation). Certaines équipes ont également décrit l’association de l’embolisation avec la perfusion in situ de chimiothérapie, ou même de véritables chimioembolisations aux particules chargées.
La cimentoplastie percutanée correspond à l’injection sous guidage de l’imagerie de polyméthylméthacrylates dans une lésion osseuse lytique douloureuse et/ou à risque fracturaire. Elle permet un effet antalgique rapide dans plus de 80 % des cas par stabilisation des foyers de microfracture et destruction thermique des nocicepteurs (peut atteindre une température de 75 °C). Réalisée sous anesthésie générale ou sédation consciente, sous guidage fluoroscopique ou scanographique, elle peut être effectuée seule dans les zones où les forces de compression prédominent (rachis, condyles fémoraux, cotyles), mais doit être associée dans les os longs (forces de torsion) à d’autres techniques de consolidation, comme l’enclouage chirurgical ou l’ostéosynthèse percutanée. La morbidité est faible (moins de 1 % de complications graves), dominée par les fuites épidurales (risque neurologique) et veineuses (risque embolique).
Figure 3. Embolisation d’hémostase : exemple d’un patient présentant des hémorragies digestives récidivantes en lien avec une volumineuse infiltration tumorale de la paroi gastrique secondaire d’un mélanome. A : hélice scanographique en reconstruction coronale montrant un épaississement circonférentiel hypervasculaire de la paroi gastrique (flèches). B : artériographie gastrique gauche initiale montrant une hypervascularisation de la paroi gastrique. C : artériographie gastrique gauche de contrôle après embolisation à la colle diluée au lipiodol.
Gestion des épanchements récidivants
Les épanchements pleuraux ou péritonéaux sont très fréquents en contexte néoplasique, avec une morbi-mortalité considérable en l’absence de traitement. Ils sont le plus souvent en lien avec des lésions de carcinose pleurale ou péritonéale, mais d’autres mécanismes peuvent être mis en cause (hypertension portale, insuffisance cardiaque, etc.). La ponction évacuatrice ou le drainage itératif de ces épanchements est simple, sûr et rapidement efficace pour soulager les symptômes, mais la récidive est quasi-constante en l’absence de traitement étiologique. Ces interventions sont facilement réalisables sous anesthésie locale, au lit du patient, avec ou sans guidage échographique, et est responsable d’une faible morbidité (hémorragie, surinfection, plaie d’organe). La pose de drain tunnelisé est une option intéressante pour la prise en charge de ces épanchements récidivants en contexte palliatif. La portion du cathéter tunnelisée sous la peau est munie d’un petit manchon favorisant la fibrose des tissus environnants. Ainsi, les risques d’infection, de fuite et de migration du drain sont beaucoup plus faibles, autorisant à laisser ce type de dispositif en place bien plus longtemps qu’un drain classique(6). Le shunt péritonéoveineux peut être utilisé dans les ascites réfractaires, y compris malignes. Cette technique consiste à raccorder un drain péritonéal et un cathéter placé dans la veine cave supérieur par voie jugulaire à l’aide d’un système à valve unidirectionnel connecté à une pompe (Denver shunt). Plus morbide que le drainage simple ou le drainage tunnelisé, il doit être réservé à des cas sélectionnés. Enfin, le stenting du canal thoracique est une technique récente en cours d’évaluation dans les ascites réfractaires sur hypertension portale.
Gestion des obstructions
• Biliaire
L’obstruction biliaire en contexte néoplasique peut s’observer dans les lésions hépatobiliaires primitives ou secondaires. Non traitée, ces manifestations cliniques (douleur, ictère, infection, dégradation de la fonction hépatique) sont communément responsables d’un inconfort, d’un affaiblissement, voire du décès rapide du patient(7). La dérivation biliaire doit donc être proposée rapidement, si l’état clinique du patient le permet, par voie endoscopique si possible, sinon par voie radiologique percutanée avec accès biliaire transpariétal sous contrôle échographique (ou fluoroscopique). La dérivation biliaire radiologique peut reposer sur la mise en place de drains plastiques multiperforés ou de stentsmétalliques autoexpansibles. Les drains plastiques peuvent être soit externes si la sténose ne peut être franchie, mais idéalement plutôt interne-externes, ces derniers ayant l’avantage de limiter les carences induites par l’externalisation complète de la bile, et d’éviter aux patients le port d’une poche de drainage. Les drains ont également l’avantage de pouvoir être changés facilement sous anesthésie locale. En revanche, en raison de calibres plus larges, les stents ont une perméabilité supérieure et permettent une internalisation complète de la bile sans dispositif externe potentiellement inconfortable pour le patient.
• Urinaire
L’obstruction urinaire peut être observée dans les néoplasies pelviennes (vésicales, gynécologiques, colorectales) ou dans les lésions tumorales rétropéritonéales primitives ou secondaires. La dérivation urinaire de ces obstructions repose en première intention sur le traitement endoscopique par pose de sonde JJ. En cas d’échec, la néphrostomie percutanée est une alternative simple, généralement sous guidage échographique/fluoroscopique. L’abord percutané peut également être complété par la pose d’un stent urétéral.
• Digestive
Certaines lésions tumorales digestives ou péritonéales peuvent être responsables de syndromes occlusifs extrêmement invalidants. La pose d’une sonde nasogastrique est le premier geste de dérivation à envisager mais ne doit pas être laissée à long terme en raison du risque de « syndrome de la sonde nasogastrique » avec complications respiratoires secondaires aux lésions laryngées au contact du tube. Il est ainsi recommandé de préférer les tubes digestifs insérés par voie percutanée, tels que les gastrostomies, gastrojéjunostomies ou jéjunostomies. Ces dispositifs peuvent être mis en place sous contrôle fluoroscopique ou échographique, et permettent une décompression digestive rapide et sûre.
Gestion des hémorragies réfractaires
Les manifestations hémorragiques sont une complication fréquente, survenant jusqu’à 10 % chez des patients atteints d’un cancer avancé. Les mécanismes lésionnels varient, de la lésion vasculaire directe par invasion tumorale, favorisée par les remaniements nécrotiques des tumeurs déjà traitées (par chirurgie, radiothérapie ou chimiothérapie), aux lésions microvasculaires par rupture de néovaisseaux tumoraux. De multiples tumeurs sont susceptibles de provoquer des hémorragies réfractaires, parmi lesquelles on peut citer les tumeurs bronchopulmonaires (hémoptysies), les tumeurs de l’appareil urinaire (hématurie), les tumeurs gastro-intestinales (hémorragie digestive haute ou basse), les tumeurs gynécologiques (hémorragie génitale), les tumeurs hépatiques (hémopéritoine)(8). Les options thérapeutiques pour la prise en charge de ces saignements doivent être discutées en fonction de l’espérance de vie et du statut fonctionnel du patient. La balance bénéfice/risque de la chirurgie ouverte dans le contexte palliatif est souvent défavorable. La prise en charge endoscopique est une option potentiellement utile mais limitée aux tumeurs gastrointestinales, bronchopulmonaires ou vésicales, avec un contrôle obtenu par cautérisation vasculaire ou par injection de sclérosants ou de vasoconstricteurs. La radiothérapie externe a également montré une efficacité hémostatique mais peut être limitée par les antécédents d’irradiation de certaines tumeurs et par un délai d’efficacité retardé. L’embolisation est ainsi devenue un traitement de première ligne chez un nombre croissant de patients avec hémorragies tumorales réfractaires. En fonction du mécanisme lésionnel, elle peut consister en l’exclusion d’une lésion vasculaire endoscopique par agent mécanique (plugs ou coils) ou liquide (colle, onyx), ou alors reposer sur la dévascularisation d’une lésion tumorale hypervasculaire par injection d’un agent liquide (microparticules, colle, voire gélatine).
*1 Service de radiologie diagnostique et interventionnelle, CHU de Nantes
2 Service de radiologie interventionnelle, Institut de cancérologie de l’Ouest
3 Équipe mobile de soins palliatifs, CHU de Nantes
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :